Imaging della BPCO: verso nuovi paradigmi diagnostici
Giovacchino Pedicelli, Pasquale Ialongo, Franco Quagliarini
Azienda Ospedaliera S.Camillo-Forlanini. UOC Radiologia Forlanini - P.zza Forlanini, 1 - 00151 Roma.
Riassunto. Negli ultimi 15 anni la diagnostica per immagini, in particolare la TC, ha contribuito a far uscire dalle nebbie del passato la diagnostica della BPCO. Nel concreto essa ha fornito nuovi strumenti di diagnosi, di valutazione quantitativa anche distrettuale e criteri di attribuzione topografica precisi, affidabili e spesso ottenibili con procedure automatiche sganciate dalla valutazione soggettiva dell’operatore. Si può ben dire che l’attuale imaging della BPCO costituisce il vero gold-standard di riferimento clinico in vivo, sostituendo completamente , e con enormi vantaggi, il riferimento autoptico del passato. L’imaging attuale ha perciò consentito di rivalutare l’opportunità clinica di riproporre nell’ambito della BPCO il criterio di selezionare i pazienti per fenotipi clinico-patologici al fine di adottare terapie personalizzate. Infine, è evidente il ruolo strategico di guida morfo-funzionale che l’imaging attuale può offrire al trattamento invasivo della BPCO.
Parole chiave: BPCO, enfisema, bronchite cronica, air-trapping.
Abstract. Over the past 15 years diagnostic imaging, in particular CT, has contributed to get BPCO diagnostic out of the mists of the past. Specifically it provided new tools for diagnosis, quantitative assessment - also detailed and district topographic criteria - reliable and often obtainable with automatic procedures free from the subjective assessment of the operator. You can say that current imaging of COPD is the true gold-standard of clinical in vivo, replacing completely, and with enormous advantages, the autopsy , which was the reference of the past. Current imaging has therefore allowed to re-evaluate the clinical appropriateness of reproposing, in the COPD context, the selection criterion for patients by clinical-pathological phenotypes, in order to adopt personalized therapies. Finally, it is evident the driving strategic role that current morpho-functional imaging can offer to BPCO invasive treatment.
Key words :COPD, emphysema, chronic bronchitis, air-trapping.
Sarà utile ricordare che il polmone è soggetto ad un declino fisiologico con progressiva riduzione di
elasticità e quindi , altrettanto progressiva, naturale perdita della funzione ventilatoria che condiziona i parametri funzionale di normalità.. Si stima che dopo i 30 anni il soggetto normale vada incontro ad una perdita di circa 30 ml/anno del FEV1 (Forced Espiratory Volume at 1st sec). Nel fumatore tale declino è accelerato, con una perdita di circa 60 ml/anno; ma il declino funzionale del fumatore non è lineare, ad esso contribuiscono fortemente i cosiddetti fattori genetici di suscettibilità.
L’espressione Bronco-Pneumopatia Cronica Ostruttiva (BPCO) raggruppa un ventaglio di condizioni patologiche sostenute dalla distruzione degenerativa del parenchima polmonare (enfisema) e dalla flogosi bronchiale , variamente combinate tra loro, accompagnate da limitazione al flusso aereo mai completamente reversibile (diversamente dall’asma).
Il processo degenerativo è fortemente favorito ed accelerato dalla inalazione di fumo di tabacco, dallo smog e altri gas nocivi. Peraltro, soltanto il 15% dei fumatori sviluppa una BPCO. Per questa e per diverse altre ragioni convincenti, si va configurando un importante ruolo di fattori genetici di suscettibilità non ancora identificati, nei confronti dei quali si vanno sviluppando diversi programmi di ricerca con elevato impegno economico internazionale.
Sia la morbilità che la mortalità per BPCO sono in forte e costante incremento nei paesi industrializzati. Si stima che, per il decennio 2020-2030, tale incremento, cui hanno contribuito negli ultimi decenni lo smog e l’abitudine al fumo delle donne, porterà la BPCO rispettivamente al quinto e al terzo posto rispetto a tutte le altre malattie. La stima per l’Italia è di circa 3 milioni di malati; nel mondo la BPCO è responsabile di circa 4 morti al minuto!
Attualmente la gravità della malattia viene stimata con la spirometria e valutata quale percentuale di riduzione del FEV1 secondo i criteri GOLD (Global Iniziative for Chronic Obstructive Lung Disease) pur nella consapevolezza che tale parametro funzionale non descrive adeguatamente la complessità della malattia né il rischio di morte. I criteri GOLD prevedono cinque gradi evolutivi, a partire dal grado zero:
è interessante sottolineare che al GOLD-0 il FEV1 è normale per definizione; in realtà a livello anatomo-patologico è già iniziata una significativa perdita di elasticità e/o della clearance bronchiale che, con gli studi radiologici (HRCT), può essere documentata sotto forma di enfisema e di air-trapping, sebbene di estensione limitata. Eventuali studi longitudinali condotti sui grossi numeri potrebbero ragionevolmente cogliere questa opportunità di diagnosi precoce per meglio comprendere la storia naturale della malattia e per proporre provvedimenti atti a modificarne favorevolmente l’evoluzione.
La BPCO è caratterizzata da spiccata eterogeneità a diversi livelli: anatomo-patologico (reperto di enfisema, bronchite cronica, flogosi e rimodellamento bronchiolare, fibrosi), clinico (dispnea, tosse, catarro, aspetto magro/pletorico), temporale (diverso grado di severità correlato con la storia naturale, esacerbazioni), spaziale ( interessamento di diverse regioni polmonari con diversa prognosi). La configurazione di malattia eterogenea rende molto complesso l’approccio diagnostico e terapeutico. Per questa ragione, già nella metà del secolo scorso (simposio Ciba del 1959) erano stati fatti importanti sforzi tesi a definire il più adeguatamente possibile i contenuti dell’acronimo BPCO, distinguendoli dall’asma e interpretandoli come una sovrapposizione di enfisema, bronchite cronica e sottotipi di asma potenzialmente riconducibili ai primi due. Qualche anno dopo (1) gli studi tesi alla tipizzazione dei fenotipi all’interno della BPCO portarono a risultati veramente convincenti , stimolando di conseguenza i medici di base, gli pneumologi ed i patologi ad una maggiore accuratezza diagnostica con l’obiettivo di poter adottare terapie personalizzate per ciascun paziente. La BPCO venne distinta in “fenotipo A”, caratterizzato dal reperto di enfisema, e “fenotipo B”, caratterizzato da bronchite cronica. Purtroppo, sebbene affascinante, questa distinzione che si basava su elementi clinici, radiologici, fisiopatologici e patologici , non trovò adeguata diffusione applicativa e nei decenni successivi finì sostanzialmente nell’oblio. Ciò avvenne per diverse ragioni: in primo luogo per scetticismo correlato con l’elevato numero di casi “indeterminati”; per pigrizia rispetto all’esigenza di meticolosità dell’inquadramento diagnostico; per comunicazione spesso inadeguata da parte accademica e delle scuole di insegnamento; per l’adozione delle linee GOLD, fuorvianti rispetto alla tipizzazione fenotipica; infine a causa del gold-standard di riferimento: quello indicato dalla tipizzazione per fenotipi era costituito dall’anatomia patologica, certamente non utilizzabile nella pratica clinica!
Il ritorno d’interesse ai fenotipi clinici della BPCO si è sviluppato di pari passo con i progressi compiuti dall’imaging negli ultimi 15 anni. La disponibilità della TC spirale e soprattutto la messa a punto della TC ad alta risoluzione (High Resolution CT) hanno segnato lo start dei nuovi modelli di studio del polmone in vivo, consentendo innanzitutto l’identificazione e la tipizzazione dell’enfisema anche nelle sue fasi iniziali, non accompagnate da significative alterazioni dei parametri funzionali. La più recente disponibilità di acquisizione volumetrica veloce delle immagini (l’intero torace in una sola apnea), con successiva ricostruzione anatomica su qualunque piano dello spazio, ha creato lo strumento per effettuare in vivo accurate valutazioni morfologiche, quantitative e topografiche dell’enfisema, ben correlabili con le modificazione dei parametri funzionali! Anche lo studio delle vie aeree, per la valutazione della flogosi bronchiale, ha raggiunto livelli di grande raffinatezza ma i dati quantitativi ottenibili con la valutazione del rapporto fra spessore della parete e lume bronchiale – pur avendo suscitato entusiasmi (2)– non si rivelano al momento , affidabili per una corretta valutazione dell’entità della flogosi e soprattutto dell’ostacolo imposto al flusso aereo. In particolar modo mancano, al momento attuale, idonei software di ricostruzione anatomica delle piccole vie aeree (< 2 mm di diametro) e delle relative valutazioni quantitative, sia morfologiche che funzionali: ciò toglie all’imaging la possibilità di valutare in modo obiettivo il punto critico della componente ostruttiva della BPCO, cioè, la flogosi bronchiolare cronica con le conseguenti alterazioni anatomo-funzionali.
Oltre ai progressi correlati con l’impiego della TC, altri importanti risultati di carattere prevalentemente funzionali sono stata raggiunti con la Risonanza Magnetica (RM) nella valutazione morfologica e quantitativa dei parametri di ventilazione, perfusione e diffusione. Per il parametro di per fusione si sono sviluppate nuove tecniche di “perfusion-CT” con gli scanner dotati di doppia sorgente “dual energy” e stanno entrando nella pratica clinica corrente gli studi di medicina nucleare mediante scanner “SPECT-CT” (TC ad Emissione di Singolo Fotone) i cui risultati sembrano correlarsi perfettamente con i dati morfologici, topografici e quantitativi ottenuti mediante MDCT (Multi Detector Computed Tomography) . L’insieme delle attuali potenzialità dell’imaging, tradotto in termini di documentazione morfologica, quantitativa e topografica configura nuovi paradigmi diagnostici e rappresenta in modo adeguato ciò che un tempo era affidato all’anatomia patologica; con i vantaggi di essere più preciso, di operare in vivo con modalità veloci, standardizzate e il più delle volte automatiche sottraendo i risultati a possibili valutazioni soggettive dell’operatore. In buona sostanza, l’imaging attuale offre un nuovo gold-standard di riferimento da utilizzare nell’impiego clinico corrente per il più adeguato inquadramento dei fenotipi clinico-patologici della BPCO, sostituendo il vecchio gold-standard costituito dall’anatomia patologica.
Per entrare concretamente nella trattazione del ruolo attuale dell’imaging e dei nuovi paradigmi diagnostici che esso offre nella diagnostica e nell’inquadramento clinico della BPCO, è utile ricordare che essa raggruppa un ventaglio di condizioni patologiche le cui alterazioni anatomo-funzionali fondamentali sono tre: l’enfisema, la flogosi delle vie aeree, le alterazioni della perfusione polmonare causate dalle prime due. Tali alterazioni devono essere considerate come tre compartimenti che l’imaging attuale, anche se ancora imperfetto, è in grado di diagnosticare e quantificare, fornendo alla clinica dati molto più sicuri rispetto al passato e contribuendo in modo più affidabile ad un indirizzo terapeutico personalizzato in grado di rivalutare con molta accuratezza i risultati delle terapie dedicate (3).
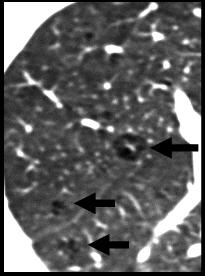
Imaging attuale dell’enfisema. L’integrità della struttura elastica del polmone è strategica per la funzione respiratoria. E’ stato confermato recentemente (4) che le pareti alveolari e le piccole vie aeree periferiche possiedono una struttura elastica comune; il processo degenerativo che colpisce questa struttura costituisce lo start della BPCO che , nella fase iniziale, si materializza visivamente nella HRCT come piccoli volumi elementari di ipertrasparenza (fig.1) dovuti sia all’iniziale distruzione del parenchima polmonare (enfisema) che al fenomeno di air-trapping correlato con il danno bronchiolare. Man mano che l’enfisema diventa più esteso e voluminoso, mediante HRCT è possibile riconoscerlo agevolmente e tipizzarne i tre tipi istologici fondamentali: centrolobulare, panlobulare, parasettale. Con l’impiego combinato di scanner veloci MDCT ad acquisizione spirale e la successiva ricostruzione panoramica delle immagini su più piani, sarà agevole individuare la perfetta localizzazione topografica. La sua quantificazione potrà essere ottenuta mediante valutazione visiva (“visual scoring”), meglio se integrata con una “density mask”; più recentemente si va diffondendo con molta efficacia la valutazione visiva e/o volumetrica mediante la documentazione dei “cluster di enfisema” che, rispetto a tutti gli altri metodi, offre la peculiarità di descriverne con molta accuratezze le caratteristiche di eterogeneità, nonché la localizzazione topografica : due dati preziosi per eventuali trattamenti invasivi.
Nell’ultimo anno si sono resi disponibili software dedicati, in grado di fornire non solo le immagini anatomiche ma anche dati quantitativi volumetrici distribuiti per polmone e per territori polmonari (superiore-medio-inferiore). Meno diffusi ma già disponibili per casi selezionati – dato i costi – vengono offerti software in grado di documentare dati quantitativi di enfisema e di ventilazione polmonare distinti per lobi e perfino per polmonari.
L’imaging della flogosi cronica delle vie aeree ha come obiettivo quello di documentare, nel modo più accurato possibile, le alterazioni morfo-funzionali delle vie aeree; in particolare l’ispessimento parietale, la riduzione del lume, la distorsione, le bronchiectasie, i segni indiretti di mortificazione della clearance bronchiale fisiologica (reperto di micronoduli con rapporto bronco-centrico, chiazze di flogosi peribronchiolare), aree di air-trapping che denunciano indirettamente la stenosi bronchiolare. Come è noto, il danno bronchiale che caratterizza la BPCO non è quello correlato con la comune bronchite cronica ma quello che investe i piccoli bronchi periferici, costituito da flogosi della parete con ispessimento e rimodellamento istologico, ostruzioni dovute all’ispessimento endoluminale e all’accumulo di secrezioni, quest’ultimo danno sfugge attualmente alla capacità di documentazione dell’imaging, anche se si vanno sviluppando in diversi centri di ricerca proposte di “surrogati” testati su bronchi di 5a e 6a generazione, in grado di dare informazioni indirette sullo stato dei bronchi più periferici, oltre la 10a generazione (5).
Non potendo, per i limiti attuali della tecnologia, documentare direttamente le strutture bronchiolari, nella pratica clinica corrente si ricorre alla dimostrazione del fenomeno dell’air-trapping per dimostrare in modo indiretto l’esistenza di stenosi flogistiche. Come è noto, tale fenomeno si enfatizza in espirazione; nella rilevazione HRCT in fase espiratoria si può assistere ad una dimostrazione caricaturale del danno funzionale, sotto forma di numerose estese aree ipodense, generalmente ben correlata con i parametri dei test funzionali (fig. 2). La rilevazione di tali quadri contribuisce moltissimo alla tipizzazione del fenotipo B. Restano spesso dubbi interpretativi delle aree ipodense, se si tratti di enfisema – che identificherebbe il fenotipo A oppure di air-trapping, a favore del fenotipo B. Possono risultare utili in questi casi l’analisi del comportamento funzionale inspiratorio-espiratorio, la disponibilità di altri parametri di riferimento dei due fenotipi quali il valore del FEV1 e la diffusione del CO.
Imaging delle alterazioni vascolari e della perfusione polmonare. Questo terzo compartimento della BPCO viene prodotto dai danni anatomici causato dall’enfisema (distruzione degenerativa del parenchima polmonare dell’enfisema) e da quelli funzionali causati dalla bronchite cronica. Questo terzo compartimento prenderà in considerazione non solo le aree o meglio i volumi dei capillari polmonari che condividono il processo distruttivo dell’enfisema, anche le grandi quantità di aree ipossiche causate da capillari compressi, dal vasospasmo permanente dovuto a carenze di ventilazione, da ispessimento e rimodellamento flogistico della parete vasale. Una grande lezione, per la comprensione di questo argomento, ci deriva dai pazienti affetti dalla sindrome Swyer-James (o di McLeod). E’ una lezione di fisiopatologia basata sullo stretto rapporto esistente fra ventilazione e perfusione: nei territori polmonari mal ventilati non può esistere adeguata perfusione poiché il flusso proveniente dall’arteria polmonare viene naturalmente deviata verso i territori ben ventilati! E’ una legge naturale di economia funzionale! Questa legge viene applicata in modo vistoso da madre natura nella BPCO. La diagnostica radiologica ne è a conoscenza dagli anni ’50 del secolo scorso quando, fra i segni radiologici rilevabili alla radiografia del torace, ne venivano annoverati con grande risalto almeno due molto affidabili costituiti da: riduzione della vascolarità periferica del polmone interessato, incremento della porzione prossimale dell’arteria polmonare e contestuale caduta di calibro delle sue diramazioni periferiche, a testimonianza dell’instaurarsi di una progressiva ipertensione del piccolo circolo, conseguenza della riduzione del letto capillare fino all’esaurimento dei territori di riserva Nei decenni 1950-1960 furono condotti adeguati studi angiografici a dimostrazione di quanto descritto.
La raffinatezza delle attuali metodologie di imaging consente, molto più agevolmente e velocemente, una documentazione visiva anche quantitativa, volumetrica e topografica della distribuzione dei rispettivi territori di ipo/iper-perfusione. Già la documentazione densitometrica di base , fornita dalla semplice HRCT senza mezzo di contrasto (fig.3 ) è in grado di fornire preziose informazioni. Bisogna dire che la ricchezza di contenuti di questa metodologia non è adeguatamente valorizzata dai radiologi sul piano clinico, forse per pigrizia culturale. Per cui si ricorre a metodologie d’impatto più vistoso, prima fra tutte la scintigrafia perfusionale. Questa metodologia, tuttora la più diffusa al mondo per studi di perfusione, fornisce corrette informazioni circa la sede, la distribuzione topografica e l’entità del danno funzionale. Peraltro, essa difetta nella risoluzione spaziale e non è in grado di contribuire a definire le cause del difetto perfusionale. Molto più adeguata appare la documentazione fornita dagli attuali scanner SPECT-CT che, in una immagine di fusione, sono in grado di mostrare l’area del difetto perfusionale nel contesto della patologia polmonare che può averlo generato. Di fatto, anche nei nostri studi preliminari le alterazioni perfusionali rilevate con la SPECT-CT appaiono perfettamente coerenti con i dati morfologici forniti dalla HRCT, con la tipizzazione dell’enfisema effettuata mediante il software di rilevazione dei “cluster di enfisema” e con i dati volumetrici quantitativi anche distrettuali. Purtroppo, per loro natura, i dati funzionali forniti dai test funzionali spirometrici non sono utilizzabili per le valutazioni comparative distrettuali ma solo nel loro significato clinico globale.
Non ci soffermiamo, in questo breve rapporto, a descrivere il formidabile contributo che la RM può portare alle valutazioni funzionali della BPCO; specificamente le valutazioni di perfusione, ventilazione e di diffusione possono essere effettuate con grande accuratezza anche distrettuale. Al momento attuale l’impiego clinico routinario della metodica è frenato dai costi eccessivi, dalla scarsa disponibilità di tecnologia e di personale specializzato. Ma in futuro, tenuto conto anche della esigenza di frequenti controlli cui sono sottoposti i pazienti affetti da BPCO, le caratteristiche non ionizzanti della metodologia contribuiscono ad una sua maggiore diffusione pratica.
Studi recenti (5) suggeriscono che le alterazioni vascolari che si sviluppano nella BPCO sono strettamente correlate con una disfunzione endoteliale indotta nell’enfisema. In particolare è stato dimostrato che il blocco di ricettori per il VEGF ( Vascular Endothelia Growth Factor) può provocare contemporaneamente l’enfisema e l’amputazione delle strutture vascolari periferiche. Se venissero confermate le conclusioni degli studi riportati bisognerebbe rivedere almeno gran parte della patogenesi delle alterazioni vascolari correlate con la BPCO: esse andrebbero viste come alterazioni primitive, non secondarie all’enfisema e quindi parte integrante dell’attuale mistero del meccanismo degenerativo con cui l’enfisema distrugge il polmone. Resterebbe invece secondario il danno vascolare indotto dall’ostruzione, strettamente correlato con il difetto di ventilazione. Pertanto, anche nella valutazione del compartimento vascolare, sembra ipotizzabile una netta differenza patogenetica fra i due fenotipi. Purtroppo la probabile correlazione fra alterazioni morfologiche dei piccoli vasi polmonari e l’estensione dell’enfisema non sono mai state sufficientemente valutate in vivo.
Conclusioni. Quanto descritto sinteticamente vuole dimostrare che negli ultimi 15 anni la diagnostica per immagini, in particolare la TC, ha contribuito a far uscire dalle nebbie del passato la diagnostica della BPCO. Nel concreto essa ha fornito nuovi strumenti di diagnosi, di valutazione quantitativa anche distrettuale e criteri di attribuzione topografica precisi, affidabili e spesso ottenibili con procedure automatiche sganciate dalla valutazione soggettiva dell’operatore. Si può ben dire che l’attuale imaging della BPCO costituisce il vero gold-standard di riferimento clinico in vivo, sostituendo completamente , e con enormi vantaggi, il riferimento autoptico del passato. L’imaging attuale ha perciò consentito di rivalutare l’opportunità clinica di riproporre nell’ambito della BPCO il criterio di selezionare i pazienti per fenotipi clinico-patologici al fine di adottare terapie personalizzate.
Infine, è evidente il ruolo strategico di guida morfo-funzionale che l’imaging attuale può offrire al trattamento invasivo della BPCO.


Fig.. 1 – HRCT del torace, selezione di una piccola aea.
Le frecce indicano minuscoli volumi di enfisema
centrolobulare in formazione, in una fase precoce,
pre-clinica e con parametri funzionali normali
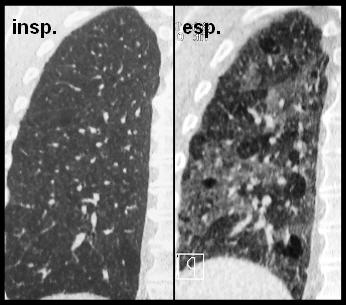 Fig.
2 – HRCT del torace in acquisizione volumetrica e ricostruzione coronale
nelle fasi di inspirazione ed espirazione. Nella fase inspiratoria si apprezza
modesta disomogeneità del parenchima polmonare con ipodensità prevalentemente
basale (enfisema). In espirazione vengono esaltate le numerose aree ipodense
correlate con il fenomeno dell’air-trapping, espressione di patologia ostruttiva
bronchiolare.
Fig.
2 – HRCT del torace in acquisizione volumetrica e ricostruzione coronale
nelle fasi di inspirazione ed espirazione. Nella fase inspiratoria si apprezza
modesta disomogeneità del parenchima polmonare con ipodensità prevalentemente
basale (enfisema). In espirazione vengono esaltate le numerose aree ipodense
correlate con il fenomeno dell’air-trapping, espressione di patologia ostruttiva
bronchiolare.
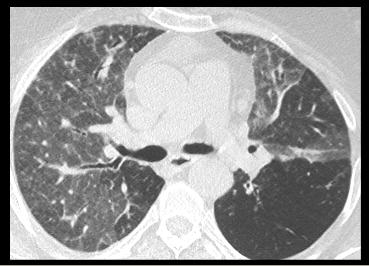 Fig.
3 – HRCT del torace in un caso di sindrome di Swyer-James. Le aree ipodense,
nettamente prevalenti a sinistra, sono correlate con air-trapping, enfisema
parafibrotico e con oligoemia da vasospasmo ipossico permanente. Il sangue
capillare viene deviato verso i territori polmonari ben ventilati che presentano
un valore densitometrico più elevato rispetto al normale.
Fig.
3 – HRCT del torace in un caso di sindrome di Swyer-James. Le aree ipodense,
nettamente prevalenti a sinistra, sono correlate con air-trapping, enfisema
parafibrotico e con oligoemia da vasospasmo ipossico permanente. Il sangue
capillare viene deviato verso i territori polmonari ben ventilati che presentano
un valore densitometrico più elevato rispetto al normale.
Bibliografia
1) B. Burrows , C.M. Fletcher , B.E. Heard et al., Emphysematous and bronchial types of chronic airways obstruction. A clinicopathological study of patients in London and Chicago. Lancet. 1966 Apr 16;1(7442):830-5.
2) Y. Nakano, C. J.Wong, Pim A. de Jong et al. The prediction of small airway dimensions using computed tomography. Am J Respir Crit Care Med, 2005, 171:142–6.
3) M. Pistolesi, Beyond airflow limitation: another look at COPD. Thorax Jan 2009, vol 64; 1
4) P. Black, P. S. T. Ching, B. Beaumont et al., Changes in elastic fibres in the small airways and alveoli in COPD. Eur Respir J 2008; 31:998-1004.
5) Shin Matsuoka, G. R. Washko, M. T. Dransfield et al., Quantitative CT Measurement of Cross-sectional Area of Small Pulmonary Vessel in COPD: Correlations with Emphysema and Airflow Limitation, Acad Radiol 2010; 17:93–99.